
Selon les articles R5212-27 et R5212-27-1 du Code de la Santé Publique, les modalités de contrôle sont définies par le directeur général de l’ANSM pour chaque type de dispositif. Ces décisions peuvent concerner :
Ces décisions sont rendues publiques sur le site de l’ANSM.
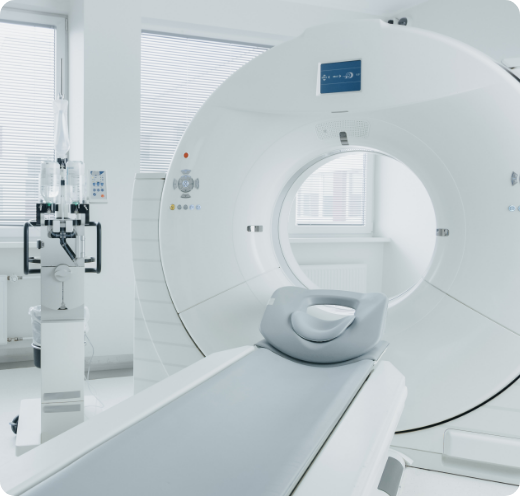
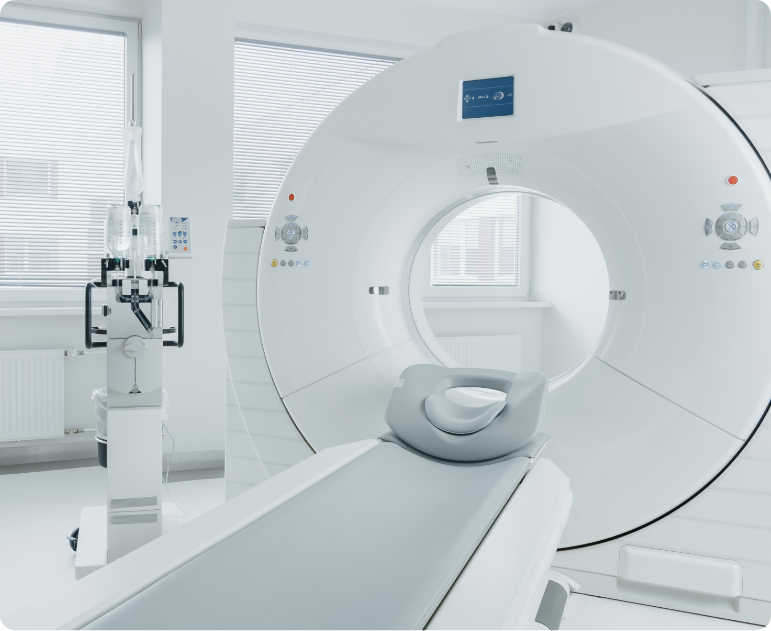
Pour les dispositifs émettant des rayonnements ionisants (par exemple les appareils de radiologie, de radiothérapie ou de médecine nucléaire), des dispositions spécifiques s’appliquent. Les décisions de contrôle sont prises en concertation avec l’Autorité de sûreté nucléaire (ASN), et les fabricants sont tenus de fournir les modalités de contrôle qualité interne. Lorsque aucune décision spécifique n’a été prise pour un dispositif, l’exploitant doit suivre les recommandations du fabricant pour le contrôle qualité.
L’exploitant d’un dispositif médical est légalement responsable de la mise en œuvre des contrôles de qualité interne et externe, selon la périodicité et les modalités fixées par l’ANSM. En l’absence de conformité, l’ANSM peut exiger que des mesures correctives soient rapidement prises.
Après chaque contrôle de qualité externe, un rapport est établi. Il contient :
Ce rapport est consigné dans le registre de traçabilité des opérations de maintenance et de contrôle.
Depuis septembre 2006, toutes les installations de mammographie numérique utilisées pour le dépistage et le diagnostic sont soumises à des contrôles de qualité externes. Ces contrôles garantissent la précision et la sécurité des examens.
Depuis mars 2009, toutes les installations de radiodiagnostic doivent subir des contrôles qualité, à la fois internes et externes. Les contrôles externes sont réalisés par des organismes accrédités, et vérifient notamment la conformité des rapports internes et certaines mesures spécifiques.
Depuis mars 2017, ces installations font l’objet de contrôles de qualité spécifiques, en particulier pour les procédures interventionnelles radioguidées. Les contrôles doivent être réalisés à différentes étapes de la vie du dispositif, y compris après chaque intervention technique.
Toutes les installations d’ostéodensitométrie sont soumises à un contrôle externe annuel ainsi qu’à un contrôle mensuel de la stabilité des appareils via télécontrôle.
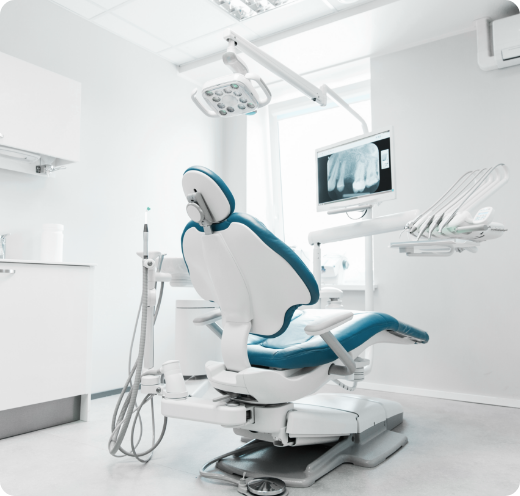
Depuis 2009, toutes les installations de radiologie dentaire doivent être soumises à un contrôle externe annuel et à un audit de contrôle interne tous les cinq ans.
Tous les scanographes doivent subir un contrôle qualité externe, qu’ils soient utilisés à des fins diagnostiques ou dans le cadre de simulations pour la radiothérapie.
Les installations de médecine nucléaire, telles que les activimètres à visée diagnostique, les sondes peropératoires et leurs électromètres associés, les compteurs gamma thyroïdiens et les caméras à scintillation, sont soumises à un contrôle qualité externe. Ce processus garantit la précision des diagnostics réalisés par ces équipements très sensibles.
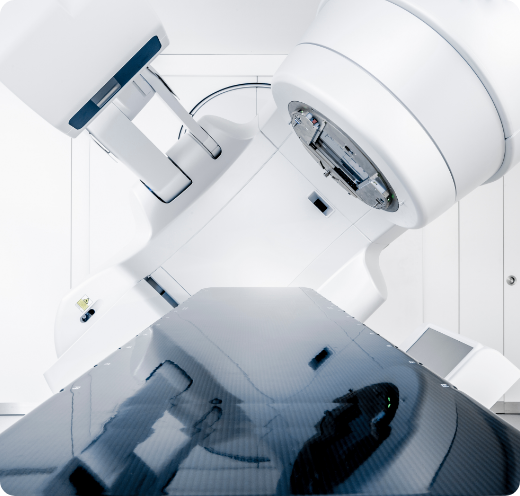
Les installations de radiothérapie externe et de radiochirurgie sont soumises à des contrôles de qualité rigoureux afin de garantir la sécurité des patients traités par rayonnement. Les décisions récentes définissent les modalités précises de ces contrôles, en réponse à l’évolution technologique des équipements.
Le contrôle qualité des dispositifs médicaux, en particulier ceux utilisés dans le domaine de l’imagerie médicale, est un processus essentiel qui garantit la sécurité des patients et l’efficacité des dispositifs. La mise en œuvre de ces contrôles, qu’ils soient internes ou externes, permet de s’assurer que les performances des dispositifs sont conformes aux standards réglementaires et aux attentes des professionnels de santé. L’exploitant d’un dispositif médical porte la responsabilité de veiller à la réalisation de ces contrôles en temps et en heure, conformément aux décisions de l’ANSM. Les organismes de contrôle accrédités, comme PAQA et CIBIO, jouent un rôle clé dans ce processus, en assurant l’impartialité et la rigueur nécessaires à l’évaluation des performances de ces équipements.